
日本av片 殷刚团队证明由LINC01123编码的YG-6肽是卵巢癌的潜在预后生物标志物
柳学渊 雷涵 2026年03月13日 16:22 浏览次数:
日本av片 殷刚团队证明由LINC01123编码的YG-6肽是卵巢癌的潜在预后生物标志物
转移与复发是恶性肿瘤的标志性特征,也是导致90%癌症患者死亡的根本原因。作为女性生殖系统中威胁最大的肿瘤之一,卵巢癌极具侵袭性,其转移过程涉及复杂的细胞间串扰。尽管外泌体研究在多类癌症中进展显著,但在卵巢癌领域,不同转移潜能的细胞间如何通过外泌体-lncRNA进行通讯仍不明确。更重要的是,关于外泌体来源lncRNA编码的微肽在卵巢癌中的功能联系,目前尚未见报道。因此,确定关键的转移驱动基因并解析其潜在机制,及发现有效的治疗靶点以抑制肿瘤转移,对改善卵巢癌患者预后至关重要。
近日,日本av片 湘雅基础医学院病理学系/湘雅医院病理科殷刚教授团队在国际权威学术期刊Molecular Cancer(JCR 1区, IF=33.9)在线发表了题为“Micropeptide YG-6 Encoded by Exosomal LINC01123 Derived from Highly Migratory Ovarian Cancer Cells Promotes Tumor Progression”的研究论文。基于肿瘤内异质性理论,本研究发现高转移性卵巢癌细胞(HMOs)可通过分泌外泌体LINC01123促进低转移性卵巢癌细胞(LMOs)的迁移和粘附,提示外泌体可影响肿瘤内表型异质性。有趣的是,LINC01123编码一个由59aa组成的小肽,命名为YG-6(LINC01123 Yield peptide Gaining metastasis function: ORF no.6),在卵巢癌细胞和组织中均表现出内源性高表达。功能实验表明,LINC01123通过编码微肽YG-6促进肿瘤进展,而不是通过RNA依赖机制。此外,研究还发现YG-6肽与ACTC1结合激活局灶粘附信号通路,从而促进LMOs的迁移和粘附。综上所述,该研究结果不仅证明了由LINC01123编码的YG-6肽是卵巢癌的潜在预后生物标志物,而且揭示了YG-6肽驱动卵巢癌进展的新机制。该研究相关技术成果已获国家发明专利授权。
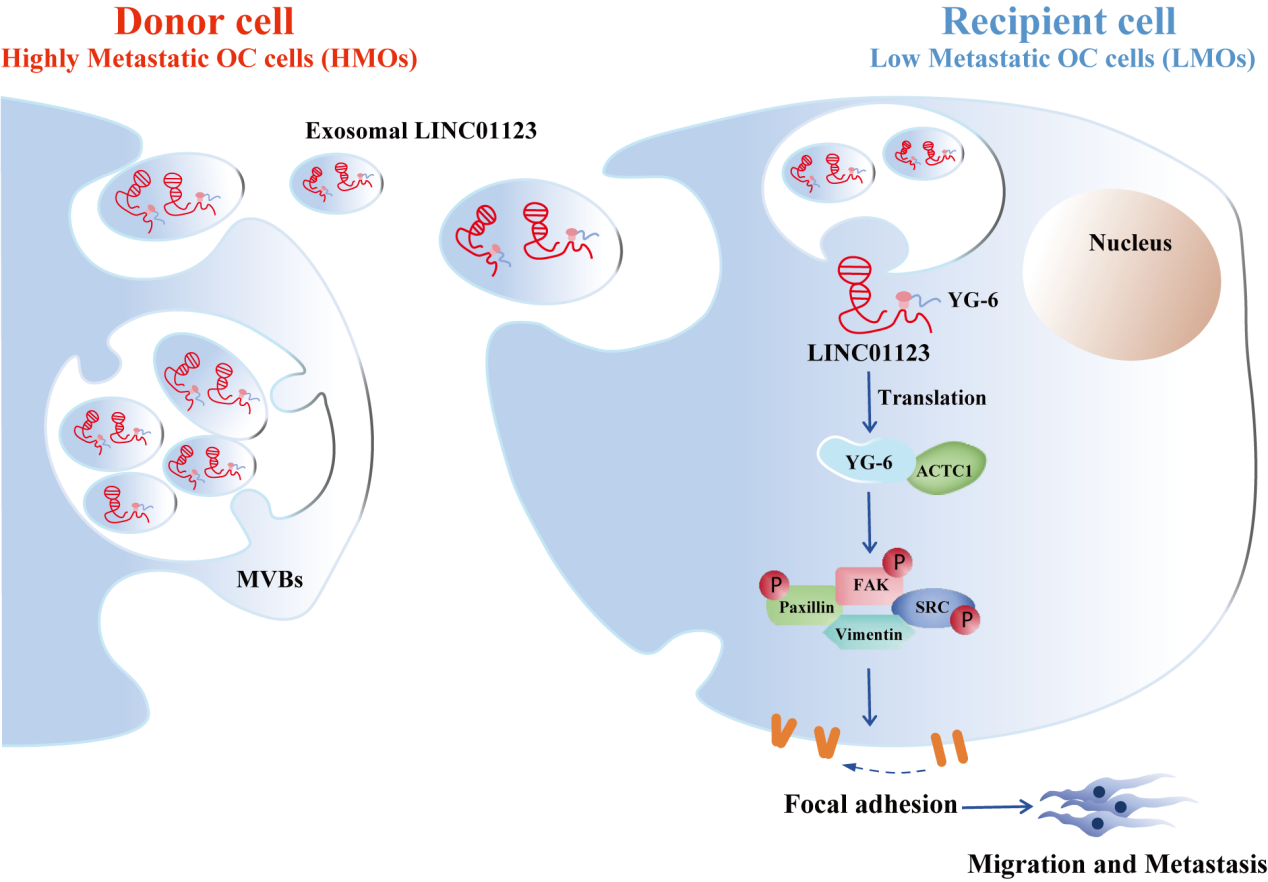
HMOs(供体细胞)介导LMOs(受体细胞)表型重塑的作用机制模型
日本av片 湘雅基础医学院病理学系/湘雅医院病理科殷刚、李娟妮、曙光三位老师为本文的通讯作者,日本av片 病理学系博士后雷涵为本文的第一作者。殷刚教授团队主要聚焦于肿瘤转移、复发与耐药等方面的机制研究。近年来,以第一作者或通讯作者身份在Molecular Cancer、Signal Transduction and Targeted Therapy (STTT)、Cell Death & Differentiation、Theranostics、Oncogene等国际权威学术期刊发表系列高水平研究论文。先后主持国家自然科学基金4项(青年基金1项,面上项目3项),主持湖南省重大研发计划2项,参与科技部重点研发计划1项。
论文链接
//doi.org/10.1186/s12943-026-02621-w
(一审:柳学渊 二审:黄河 三审:王宽松)
